Pour le développement de tout produit innovateur, nous développerons votre devis d'étude clinique, votre protocole, et vous aiderons à déterminer la taille d'échantillon «Sample Size» de votre étude, en plus d’identifier les marqueurs et les critères-cibles cliniques :
Pour le développement de produits génériques ou supergénériques, nous définirons le programme d’études de bioéquivalence approprié, incluant les études d’équivalence thérapeutique utilisant des biomarqueurs ou des marqueurs pharmacodynamiques «PD Endpoint»
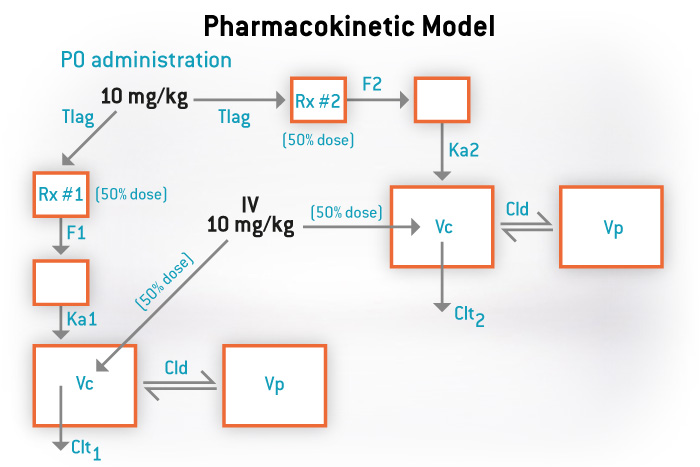
Nous répondrons également à tous vos besoins liés à la pharmacocinétique :
L&C peut également vous épauler dans la réalisation des études cliniques ou dans toutes autres études liées au développement de produits innovants, génériques ou supergénériques :
Analyses et rapports prédisant, chez diverses populations en pédiatrie, les profils de concentrations des médicaments ainsi que leur efficacité et leur toxicité
Analyses et rapports prédisant, chez des patients en insuffisance rénale, les profils de concentrations de médicaments ainsi que leur efficacité et leur toxicité